Le laboratoire LAMSI possède les agréments en PMA et pour le dépistage pré-natal de la trisomie 21.
Situé 45 boulevard Dubouchage à Nice, le Lamsi, réalise les bilans de fertilité, de spermiologie et des préparations d’inséminations artificielles intra-conjugales (IAC) dans le cadre de l’assistance médicale à la procréation (AMP).
Les entretiens préalables à l’AMP et la plupart des prélèvements des examens de biologie de la reproduction sont réalisés au Lamsi. Mais pour certains examens, comme le calcul de risque de la trisomie 21 par marqueurs sériques maternels, ou le DPNI, il est possible de se rendre sur n’importe lequel des laboratoires SYNLAB-BARLA pour réaliser le prélèvement.
Renseignez-vous auprès de votre laboratoire habituel.
Le pôle de biologie de la reproduction en détails
Les tests anténataux
Les marqueurs sériques maternels de la trisomie 21
Le dépistage de la trisomie 21 est proposé en France depuis 1997 à toutes les femmes enceintes. La trisomie 21 est l’anomalie chromosomique la plus fréquente et la première cause de retard mental. Le risque d’avoir un enfant atteint de trisomie 21 augmente avec l’âge de la mère.

Le dépistage combiné du 1er trimestre
Il s’effectue au 3ème mois de grossesse (soit entre 11 semaines et 13 semaines et 6 jours d’aménorrhée). Il s’agit du calcul d’un risque et non d’un diagnostic. Ce calcul intègre :
- les mesures échographiques de la clarté nucale (CN) et de la longueur crânio-caudale (LCC),
- les valeurs du dosage de la PAPP-A (pregnancy associated plasma protein A) et de la beta hCG libre, hormones secrétées par le placenta ou le fœtus et qui passent dans le sang maternel,
- Mais également des données maternelles (voir ci-dessous).
Dans les cas de découverte tardive de grossesse : Le dépistage du 2e trimestre
Il peut être réalisé entre 14 semaines et 17 semaines et 6 jours d’aménorrhées. Il prend en compte le dosage de la beta-HCG libre et de l’alfa-foeto-protéine, sans intégration de la CN.
A savoir
Les données de la patiente utilisées aussi dans le calcul du risque sont les suivantes : âge, origine géographique (impact notamment sur la PAPP-A), tabagisme, diabète insulino-dépendant, antécédent de T21, poids, insuffisance rénale.
Dans les cas de grossesse par don d’ovocytes, c’est l’âge de la donneuse qui entre dans le calcul du risque.
Dans le cas d’un transfert d’embryon congelé le calcul intègre l’âge de la patiente au moment de la congélation.
Dépistage HT21 en pratique
– Le prélèvement sanguin peut être réalisé dans n’importe lequel des laboratoires SYNLAB-BARLA, en respectant impérativement les dates précisées par votre médecin ou votre sage-femme.
– Les documents suivants doivent être présentés au laboratoire pour la réalisation du test :
- le formulaire comportant l’attestation de consultation, le consentement de la femme enceinte et les renseignements cliniques dûment complétés, notamment par l’échographiste : mesure de de la CN, LCC et son numéro d’affiliation au réseau de périnatalité,
- la prescription,
- la carte vitale,
- le compte-rendu d’échographie.
– Le dosage des marqueurs sériques maternels et le du calcul de risque sont réalisés sur le plateau technique de la SELAS BARLA pour le Lamsi, laboratoire agréé. Ils sont effectués avec la technologie Delfia XPress de Perkin Elmer.
– Les résultats sont rendus au prescripteur seulement, qui se charge de les communiquer à la femme enceinte.




Le dépistage prénatal non invasif (DPNI) ou test ADN libre circulant de la trisomie 21 (ADN LC T21)
L’intérêt des tests génétiques non invasifs
Ces tests analysent des fragments d’ADN fœtal issus de cellules trophoblastiques (du placenta) circulants dans le sang de la mère dès les premières semaines de grossesse (de 11 SA à la fin de la grossesse). Avec une sensibilité et une spécificité supérieures à 99 %, ils permettent d’exclure avec un très haut degré de fiabilité le diagnostic de trisomie 21chez le foetus. Ils permettent aussi de mettre en évidence une trisomie 13 ou 18.
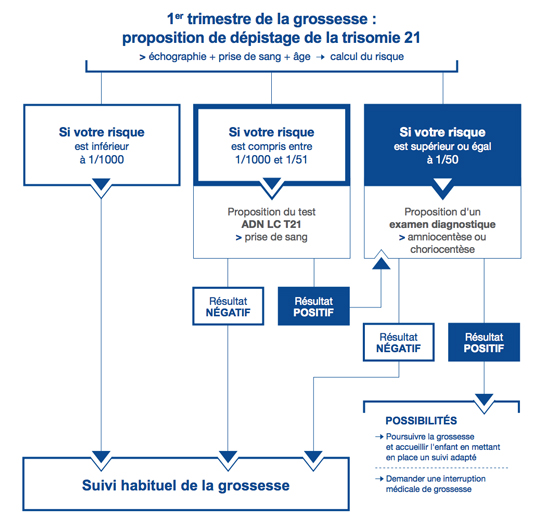
Depuis le 17/01/2019, ce test est remboursé par la sécurité sociale dans les cas suivants :
- à toutes les femmes enceintes dont le niveau de risque de trisomie 21 fœtale est compris ente 1/1000 et 1/51 à l’issue du dépistage par dosage marqueurs sériques (à titre principal, dépistage combiné du 1er trimestre).
- lors grossesse multiple,
- lors d’antécédent de grossesse avec trisomie 21 par translocation robertsonienne,
- lors d’antécédent de grossesse avec une autre aneuploïdie que la trisomie 21.
A SAVOIR :
La possibilité de réalisation d’un caryotype fœtale d’emblée soit proposée à toutes les femmes enceintes dont le niveau de risque de trisomie 21 fœtale est supérieur ou égal à 1/50 à l’issue du dépistage par dosage des marqueurs sériques (à titre principal, dépistage combiné du 1er trimestre). Mais un test DPNI pourra cependant être réalisé avant un éventuel caryotype fœtal selon la préférence de la femme enceinte.
Le DPNI en pratique
- La réalisation du DPNI nécessite de fournir au laboratoire :
- le formulaire d’attestation de consultation et de consentement de la femme enceinte,
- la feuille de renseignements cliniques complétée,
- le compte-rendu d’échographie,
- la prescription.
- Il doit être réalisé impérativement dans les dates indiquées par le prescripteur à partir de la 12e semaine d’aménorrhée et reste possible tout au long de la grossesse.
- Il est possible de se rendre à n’importe lequel des laboratoires BARLA pour réaliser le prélèvement sanguin. Les biologistes du Lamsi sont à la disposition des médecins prescripteurs pour tout renseignement sur l’intérêt de ces tests et les modalités de leur réalisation.
- Dans le réseau des laboratoires SYNLAB, le test est réalisé par le laboratoire spécialisé de génétique ALPIGENE (Lyon). Le prélèvement sanguin de la femme enceinte est transmis au l aboratoire Alpigène dans les conditions de transport adéquates.
- La technologie utilisée est NeoBona Illumina. Son coût,lorsqu’il n’est pas pris en charge par la sécurité sociale est de 390 euros.
- Il arrive que le test soit inexploitable et qu’un deuxième prélèvement soit nécessaire. Dans ce cas le test est pris en charge par la sécurité sociale.
Quand parle-t-on d’infertilité ?
L’infertilité est la difficulté pour un couple de concevoir un enfant. On parle d’infertilité quand un couple, qui n’a pas d’antécédents médicaux particuliers et qui a des relations sexuelles régulières sans contraception, est dans l’incapacité d’obtenir une grossesse après 1 an (ou 6 mois si la femme est âgée de 35 ans ou plus).
Quelles sont les causes de l’infertilité ?.
Le couple amené à consulter le gynécologue pour infécondité va bénéficier d’une exploration complète de sa fertilité afin de repérer d’éventuelles causes d’infertilité et pour choisir les meilleures solutions que peut apporter l’aide médicale à la procréation (AMP). L’âge de la conjointe est un facteur à prendre en compte sachant que la fertilité est à son maximum vers 25 ans, pour devenir quasiment nulle après 45 ans. Chaque couple présente une combinaison différente de causes éventuelles qu’il faut cartographier.
Du côté de Monsieur (30% des cas)
• Anomalie des critères spermatiques.
• Trouble de l’érection.
• Anomalie génétique : anomalies au niveau du caryotype (translocations).
• Azoospermie (sécrétoire ou excrétoire).
• Cryptozoospermie.
• Ejaculation rétrograde.
• Présence d’autoanticorps anti spermatozoïdes.
Du côté de Madame (30% des cas)
• Troubles ovulatoires c’est-à-dire incapacité à produire un ovocyte capable d’être fécondé.
• Obstruction des trompes.
• Défaut de la glaire cervicale.
• Causes endocriniennes entrainant un dérèglement hormonal : pathologie de la thyroïde, excès de prolactine etc…
• Anomalie au niveau de l’utérus : fibromes, polypes, malformations utérines.
• Facteurs vaginaux : vaginisme entrainant une impossibilité d’avoir des rapports sexuels.
Dans 30% des cas des cas, l’infertilité est d’origine mixte.
Dans 10 % des cas, l’infertilité est inexpliquée.



Quels sont les examens biologiques d’exploration de la fertilité ?
Pour Madame :
- Recherche d’une anomalie de l’ovulation (anovulation, dysovulation) par dosages hormonaux : FSH, LH, OESTRADIOL, PROLACTINE, courbe de températures, échographie.
- Evaluation de la réserve ovarienne : dosages hormonaux, notament hormone anti-müllerienne* (AMH), échographie.
- Recherche d’anomalies de la qualité de la glaire dues à des causes hormonales, infectieuses, interventionnelles (conisation). Le test de Huhner** est indiqué dans cas.
- Rechercher une anomalie génétique : caryotype (analyse du génome)
En complément des examens biologiques, l’exploration pourra comporter la recherche par échographie :
• D’une anomalie du tractus génital.
• D’une anomalie des trompes : altérées ou obturées pour différentes raisons (infections, grossesse extra-utérine).
• D’une endométriose.
*L’AMH est un marqueur direct de la réserve ovarienne et le meilleur marqueur de la réponse ovarienne à une stimulation dans le cadre d’une AMP (ce dosage est remboursé par la Sécurité sociale).
** Le test post-coïtal ou test de Hünher a pour objectif de vérifier la qualité de la glaire et la présence de spermatozoïdes dans la glaire cervicale après un rapport sexuel, mais aussi d’évaluer leur mobilité et leur survie.
Lors de la consultation, le gynécologue peut prescrire tout examen qu’il jugera nécessaire pour établir la cause de l’infertilité.
Tous les dosages hormonaux (FSH, LH, AMH etc…), toutes les recherches d’infections (prélèvements génitaux) et toutes les sérologies infectieuses (HIV, HEPATITE B, SYPHILIS etc…) sont effectués dans chacun nos laboratoires SYNLAB Barla.
Le test de HUHNER est lui réalisé uniquement au sein du laboratoire LAMSI et sur rendez-vous.
Pour Monsieur
Le bilan biologique est conduit par le gynécologue.
- Le spermogramme spermocytogramme reste chez l’homme l’examen de première intention.
- Le test de HUHNER: Simple à réaliser, il permet d’étudier l’ensemble sperme-glaire cervicale après un rapport sexuel.
- D’autres tests comme la spermoculture, la recherche d’auto-anticorps anti spermatozoïdes peuvent compléter le bilan initial.
- Le test de migration survie TMS sera effectuée pour évaluer la possibilité d’une prise en charge en PMA et choisir la technique adapté aux resultats de ce test (IIU, FIV conventionelle ou avec microinjection).
- En cas d’anomalies majeures, d’autres examens complémentaires seront pratiqués : dosages hormonaux (FSH, TESTOSTERONE, etc…).
- Une consultation auprès d’un andrologue et ou un urologue peut s’avérer nécessaire.
- Dans certains cas, l’imagerie médicale (échographie, doppler) pourra aussi apporter sa contribution au diagnostic. Ainsi qu’un conseil génétique après une exploration du génome par un caryotype).
De bonnes conditions de recueil de sperme sont indispensables à une bonne interprétation de ces examens.
Les différentes analyses du sperme (spermogramme, spermocytogramme, test de migration survie etc…) nécessitent des conditions particulières (abstinence de 3 à 5 jours, respect des recommandations fournies lors de l’accueil, etc…). Ces analyses du sperme se font exclusivement au laboratoire Lamsi et sur rendez-vous.
Ce que dit a loi :
L’arrêté du 5 octobre 2023 modifiant l’arrêté du 11 avril 2008 rend l’AMP accessible à toutes les femmes en couple avec un homme, une femme ou célibataire.
La mise en œuvre de l’AMP est indiquée lorsqu’une infertilité est diagnostiquée chez le couple. Elle se pratique dans des établissements autorisés et par des praticiens compétents. Les bilans et les soins pour infertilité peuvent être pris en charge à 100 %. Les actes de procréation médicalement assistés sont pris en charge jusqu’au 45e anniversaire de la femme, sous accord préalable.
Sont pris en charge :
Une seule insémination artificielle par cycle, avec un maximum de six pour obtenir une grossesse.
Quatre tentatives de FIV pour obtenir une grossesse.
Cependant, l’équipe médicale peut limiter ce nombre de tentatives en fonction du dossier clinico-biologique du couple.
Au laboratoire LAMSI nous pratiquons uniquement les IAC (insémination avec sperme du conjoint).
Le recours à l’AMP
Une décision pluridisciplinaire est prise à l’issue d’une consultation avec le biologiste.
Après les consultations lui ayant permis d’établir l’indication de l’IAC, le gynécologue oriente le couple vers le laboratoire LAMSI pour une consultation avec le biologiste, sur rendez-vous, uniquement.
Lors de cet entretien une information loyale, claire et appropriée est délivrée au couple lui permettant de participer à la prise en charge de son infertilité. Les entretiens portent notamment sur les motivations des futurs parents et visent à les informer sur les techniques d’AMP et leurs conséquences. Le biologiste s’assurera que les informations communiquées sont bien comprises par le couple et lui apportera les réponses à ses questions. Il lui remet une brochure à la fin de l’entretien “le guide de l’assistance médicale à la procréation”.
A noter la loi impose un délai de réflexion de 1 mois entre la consultation avec le biologiste et la 1ère insémination. Passé ce délai, le couple doit confirmer sa demande d’AMP par écrit auprès du médecin.
La constitution du dossier d’IAC
Avant la consultation avec le biologiste le secrétariat du laboratoire LAMSI vous fournira une liste des documents à apporter le jour de l’entrevue.
Liste des documents à fournir :
DOSSIER MÉDICAL
- Fiche navette bio-clinique : la ligne « indication de l’IAC » doit être complétée par votre gynécologue, et il doit dater et signer dans la marge.
- Résultats des examens sérologiques suivants, pour les deux conjoints, datant de moins de 6 mois le jour de la première IAC :
- HIV
- Hépatite C
- Hépatite B : Ag Hbs, Ac Hbs et Ac Hbc
- Syphilis
- Toxoplasmose et rubéole pour madame. Les femmes non immunisées contre la rubéole doivent procéder à une vaccination anti-rubéolique avant toute insémination. Le refus de vaccination est possible, mais doit donner lieu à un document écrit.
- Résultats d’un spermogramme et d’une spermoculture datant de moins de 6 mois.
- Résultat d’un Test de Migration-Survie des spermatozoïdes (TMS).
- Résultats d’un bilan hormonal à J2 ou J3 (Estradiol, LH et FSH). Le bilan peut comprendre le dosage de l’AMH.
- Compte-rendu d’une hystérosalpingographie.
- Comptes-rendus des tentatives d’AMP (IAC ou FIV) déjà réalisées dans d’autres centres, s‘il y en a eu.
DOSSIER ADMINISTRATIF
- Photocopies des cartes d’identité ou du passeport des deux conjoints (les documents doivent être en cours de validité lors de la démarche).
- Pour les couples mariés : photocopie du livret de famille.
- Pour les couples non mariés : certificat de concubinage (qui peut être établi par la mairie) ou attestation de vie commune.
ENTENTE PRÉALABLE
Afin d’obtenir le remboursement des IAC par l’assurance maladie, une demande d’entente préalable est nécessaire. Celle-ci est à faire signer et tamponner par votre gynécologue, puis le biologiste remplira le cadre qui lui est réservé lors de l’entretien que vous aurez avec lui.
La demande d’entente préalable doit être libellée au nom de Madame, et doit être accompagnée d’une ordonnance, également au nom de Madame, pour 6 cycles d’IAC (ou pour le nombre d’IAC restant avant la sixième).



Le suivi de l’ovulation
L’IAC, sera réalisée au pic de l’ovulation. Lorsqu’il y a stimulation, le traitement commence au 3ème ou 5ème jour du cycle. Il s’agit d’injections quotidiennes de FSH recombinante. La surveillance régulière par monitoring (toutes les 24 ou 48h) de la stimulation commence au 10ème jour du cycle : échographies réalisées par le gynécologue pour mesurer et compter les follicules et évaluer l’épaisseur de l’endomètre, et dosages sanguins de l’estradiol réalisés au laboratoire. En fonction de la qualité de la stimulation observée lors du monitoring, le traitement est adapté, au cas par cas.
Lorsque la maturation folliculaire et la stimulation sont suffisantes, celle-ci est stoppé et le gynécologue déclenche l’ovulation (par une injection de hCG recombinante ou d’un analogue du GnRH, qui miment un pic de LH).
L’IAC est alors programmée 37 à 40 heures après cette injection, au moment précis de l’ovulation.
L’IAC
Définition
L’insémination intra-utérine n’est pas une fécondation in vitro, mais c’est cependant une PMA car elle nécessite d’une part, l’intervention d’un gynécologue pour la stimulation ovarienne et l’insémination intra-utérine proprement dite et, d’autre part, l’intervention du laboratoire pour la préparation de sperme.
C’est la technique de PMA la plus simple à mettre en œuvre. Elle est effectuée au sein du laboratoire LAMSI (laboratoire autorisé par l’ARS) sous la responsabilité de biologistes compétents (agréés par l’ARS).
Comme toutes les techniques d’AMP, elle se fait uniquement sur indication médicale.
Cette technique est toujours associée à une stimulation de l’ovaire (avec surveillance échographique et bilan biologique).
Les conditions de suivi et de surveillance de la stimulation sont assurées par les gynécologues.
Elle ne modifie que très peu les habitudes de vie et reste compatible avec l’exercice d’une activité professionnelle. Comme il n’est pas toujours simple de prendre un jour de congé pour se rendre au rendez-vous obligatoire le jour de la réalisation de l’IAC, une loi récente autorise les couples à s’absenter de leur travail.
La loi n° 2016-41 du 26 janvier 2016 dans son article L1225-16.
Les indications d’IAC sont :
- Anomalies du col de l’utérus
- Glaires innapropriés (mucus cervical)
- Échecs répétés de stimulation simple de l’ovulation.
- Anomalies “modérées” du spermogramme
- Problèmes d’éjaculation (dont l’éjaculation rétrograde)
- Anomalies anatomiques (hypospadias)
- Impuissance de tout ordre : paraplégique, psychologique…
- stérilité inexpliquée, chez la femme jeune, après plusieurs essais de traitements simples.
Elle est pratiquée généralement sous deux conditions :
- Un test de migration survie des spermatozoïdes compatible avec une IAC.
- Les trompes de la conjointe doivent être perméables (avec un compte rendu de HSG le certifiant).
Déroulement de l’IAC :
Dés que le couple a connaissance de la date programmée de l’insémination, il prend rendez-vous au laboratoire LAMSI pour le recueil du sperme en vue de l’IAC. Les cartes d’identité des 2 membres du couple seront exigées par le secrétariat.
Le jour de l’insémination, monsieur devra se rendre au laboratoire lamsi pour faire le recueil du sperme par masturbation. Il aura pris soin auparavant de respecter une abstinence de 2 à 3 jours.
Après analyse du sperme, le biologiste utilisera la méthode la mieux adaptée pour réaliser la préparation à inséminer.
La préparation est ensuite remise à madame qui devra se rendre sans délai au cabinet de son gynécologue qui procèdera à l’insémination. C’est un acte non douloureux.
Après l’insémination, madame peut reprendre son activité normalement
A savoir : le déclenchement ne s’effectue que si les paramètres de la surveillance sont de bonne qualité. Dans certains cas, la réponse ovarienne est trop importante (hyperstimulation) et nécessite l’arrêt du traitement (risque de grossesse multiple). A l’opposé, l’abandon de la tentative peut être motivé par une mauvaise réponse ovarienne (hypostimulation) ou par une mauvaise réaction du sperme à la préparation (nombre de spermatozoïdes trop faible). Ces mauvaises réponses ovariennes nécessiteront une modification du protocole thérapeutique pour une tentative ultérieure.
Résulats
En cas d’absence de règles 15 jours après l’insémination une prise de sang sera nécessaire pour diagnostiquer un éventuel début de grossesse.
En cas d’échec une nouvelle tentative pourra être programmée en accord avec le gynécologue.
Les chances d’obtenir une grossesse devraient être entre 10 et 15 % par cycle de traitement. La répétition des cycles d’insémination n’aboutit pas à une addition arithmétique des chances de succès, mais augmente néanmoins celles-ci jusqu’à un maximum de 6 inséminations.